Antibiotika
(Nová stránka: {{TOCright}} '''Antibiotika''' jsou léky ničící nebo zpomalující růst baktérií. Antibiotika tvoří jednu třídu "antimikrobiálních léků" ([[antimikro...) |
|||
| (Nejsou zobrazeny 3 mezilehlé verze od 1 uživatele.) | |||
| Řádka 1: | Řádka 1: | ||
{{TOCright}} | {{TOCright}} | ||
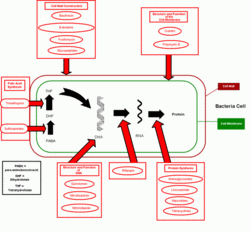
| − | '''Antibiotika''' jsou [[lék]]y ničící nebo zpomalující růst [[ | + | [[Soubor:AkceAntibiotik.gif|thumb|250px|Body působení antibiotik na bakterie.]] |
| + | '''Antibiotika''' jsou [[lék]]y ničící nebo zpomalující růst [[bakterie|bakterií]]. Antibiotika tvoří jednu třídu "antimikrobiálních léků" ([[antimikrobiotika]] nebo též bakteriostatika), větší skupina kterých též obsahuje [[antivirotika]], antiplísňové a antiparazitické léky. Jsou relativně neškodné pro hostitele a proto mohou být použity na [[léčba|léčbu]] [[infekce|infekcí]]. Termín "antibiotika" původně označoval jen formy antibiotik odvozených ze živých organismů, ale teď je aplikován i na syntetické [[antimikrobiotika]], např. [[sulfonamid]]y. Antibiotika jsou malé molekuly s molekulární hmotností méně než 2000 a nepatří mezi [[enzym]]y. | ||
| − | Na rozdíl od předešlých způsobů léčby infekcí, které obsahovali otravy jako [[strychnin]], antibiotika byli označeny jako "magické tablety" - [[lék]]y zasahující [[nemoc]] bez poškození pacienta. Antibiotika nejsou efektivní u [[virus|virových]], [[plíseň|plísňových]] a jiných | + | Na rozdíl od předešlých způsobů léčby infekcí, které obsahovali otravy jako [[strychnin]], antibiotika byli označeny jako "magické tablety" - [[lék]]y zasahující [[nemoc]] bez poškození pacienta. Antibiotika nejsou efektivní u [[virus|virových]], [[plíseň|plísňových]] a jiných nebakteriálních infekcí a jednotlivé antibiotika jsou značně odlišné ve své účinnosti na různé typy bakterií. Některé specifické antibiotika (zvané "úzko-spektrální antibiotika") zasahují buď gram-negativní nebo gram-pozitivní [[bakterie]] a jiné jsou víc ''širokospektrální'' antibiotika. Účinnost jednotlivých antibiotik se mění podle lokality infekce a schopnosti antibiotika dosáhnout dané místo. Orální (užívané ústně) antibiotika jsou nejlepším řešením, jsou-li účinné a nitrožilní antibiotika se používají ve vážnějších případech. Antibiotika mohou být někdy aplikovány místně, např. jako oční [[kapky]] nebo [[mast]]. |
== Historie == | == Historie == | ||
| − | Následujíc dřívější experimenty, které ukázaly zajímavé antibakteriální účinky z různých bakteriálních sekretů, německý vědec E. de Freudenreich izoloval v roce 1888 bakteriální sekreci a zaznamenal její antibakteriální vlastnosti. Pyocyanáze vylučována bacilem "Bacillus pyocyaneus" zpomalila růst jiných | + | Následujíc dřívější experimenty, které ukázaly zajímavé antibakteriální účinky z různých bakteriálních sekretů, německý vědec E. de Freudenreich izoloval v roce 1888 bakteriální sekreci a zaznamenal její antibakteriální vlastnosti. Pyocyanáze vylučována bacilem "Bacillus pyocyaneus" zpomalila růst jiných bakterií v okolí a byla toxická pro mnoho bakterií způsobujících [[nemoc]]. Naneštěstí vlastní toxicita pyocyanázy a její nestabilní charakter neumožnil její použití jako účinného bezpečného antibiotika v lidském těle. |
| − | První účinné objevené antibiotikum byl [[penicilin]]. Francouzský doktor Ernest Duchesne zaznamenal v roce 1896 tezi, že určité plísně druhu Penicilium ničí bakterie. Duchesne skonal během několika let a jeho výzkum byl zapomenut po generaci, až do přispění náhody. [[Alexander Fleming]] pěstoval bakterie na agarových plotnách a jedna z nich byla napadena náhodní plísňovou kontaminací. Fleming zaznamenal čistou zónu kolem kolonie [[plíseň|plísně]]. Protože Fleming předtím studoval schopnost enzymu [[lysozym]] ničit | + | První účinné objevené antibiotikum byl [[penicilin]]. Francouzský doktor Ernest Duchesne zaznamenal v roce 1896 tezi, že určité plísně druhu Penicilium ničí bakterie. Duchesne skonal během několika let a jeho výzkum byl zapomenut po generaci, až do přispění náhody. [[Alexander Fleming]] pěstoval bakterie na agarových plotnách a jedna z nich byla napadena náhodní plísňovou kontaminací. Fleming zaznamenal čistou zónu kolem kolonie [[plíseň|plísně]]. Protože Fleming předtím studoval schopnost enzymu [[lysozym]] ničit bakterie, teď pochopil, že [[plíseň]] vylučovala něco, co zastavilo růst bakterií. Věděl, že tato látka může mít obrovský užitek pro medicínu. I když nebyl schopen rafinovat (očistit) sloučeninu (kruh beta-laktam v penicilinové molekule nebyl stabilní po vyzkoušených rafinačních metodách), popsal objev ve vědecké literatuře v roce 1929. Protože [[plíseň]] byla druhu ''Penicilium'', nazval tuto sloučeninu penicilin. |
V 30. letech 20. století německý výzkumník Gerhard Domagk zkoumal antibakteriální vlastnosti některých barviv. Jedním z nich byl [[sulfonamid]], ''prontosil'', který se ukázal být účinným proti infekcím u lidí pro svoji proměnu v hostitelu na aktivní formu - ''sulfanilimid''. Podle současné širší definice to možno asi kvalifikovat jako první úspěšné použití orálního (ústního) antibiotika. Po nějaké době Rene Dubos izoloval ''[[tyrotricin]]'' - antibiotikum používané místně na kožní infekce z půdních bakterií. | V 30. letech 20. století německý výzkumník Gerhard Domagk zkoumal antibakteriální vlastnosti některých barviv. Jedním z nich byl [[sulfonamid]], ''prontosil'', který se ukázal být účinným proti infekcím u lidí pro svoji proměnu v hostitelu na aktivní formu - ''sulfanilimid''. Podle současné širší definice to možno asi kvalifikovat jako první úspěšné použití orálního (ústního) antibiotika. Po nějaké době Rene Dubos izoloval ''[[tyrotricin]]'' - antibiotikum používané místně na kožní infekce z půdních bakterií. | ||
| Řádka 13: | Řádka 14: | ||
Pro zvýšenou potřebu léčby infekcí z ran ve 1940-tych letech bylo mnoho prostředků vloženo do výzkumu a rafinace penicilinu a team, který vedl Howard Walter Florey, úspěšně vyprodukoval použitelná množství rafinované aktivní složky, která byla rychle testována na klinických případech. Doktoři byli překvapeni z rychlé a spolehlivé léčby stavů, které do té doby byly těžce léčitelné a často fatální. Výzkum dalších druhů plísní a jiných organismů ukázal až dosud neznámou úrověň chemického boje proti bakteriím. Nové antibiotika byly rychle objevovány a začali se široce používat. Nová éra výzkumu podobných "magických" chemoterapeutických léčiv pro jiné nemoci eventuálně vedla k úspěchům v [[rakovina|rakovinové]] chemoterapii. | Pro zvýšenou potřebu léčby infekcí z ran ve 1940-tych letech bylo mnoho prostředků vloženo do výzkumu a rafinace penicilinu a team, který vedl Howard Walter Florey, úspěšně vyprodukoval použitelná množství rafinované aktivní složky, která byla rychle testována na klinických případech. Doktoři byli překvapeni z rychlé a spolehlivé léčby stavů, které do té doby byly těžce léčitelné a často fatální. Výzkum dalších druhů plísní a jiných organismů ukázal až dosud neznámou úrověň chemického boje proti bakteriím. Nové antibiotika byly rychle objevovány a začali se široce používat. Nová éra výzkumu podobných "magických" chemoterapeutických léčiv pro jiné nemoci eventuálně vedla k úspěchům v [[rakovina|rakovinové]] chemoterapii. | ||
| − | Objev antibiotik spolu s [[anestezie|anestezií]] a aplikací [[ | + | Objev antibiotik spolu s [[anestezie|anestezií]] a aplikací [[hygiena|hygienických praktik]] u [[doktor]]ů (např. mytí rukou a použití sterilizovaných instrumentů) značně inovoval [[medicína|medicínu]]. Považuje se za největší progres pro [[zdraví]] od moderní kanalizace. Lidé v rozvojových zemích si těžko dovedou představit, že jedno škrábnutí vždy nese risk [[infekce]] a skonu. |
==Klasifikace== | ==Klasifikace== | ||
| Řádka 102: | Řádka 103: | ||
==Vedlejší efekty== | ==Vedlejší efekty== | ||
| − | Vedlejší efekty jsou v rozsahu od slabé [[bolest]]i hlavy po vážné alergické reakce. Jeden z častějších vedlejších efektů je [[průjem]], který rezultuje z narušené rovnováhy [[střevo|střevní]] flóry, "dobrých bakterií", které přebývají v zažívacím systému člověka. Jiné vedlejší efekty mohou rezultovat z interakce mezi antibiotikem a jinými léky, např. zvýšený risk poškození [[ | + | Vedlejší efekty jsou v rozsahu od slabé [[bolest]]i hlavy po vážné alergické reakce. Jeden z častějších vedlejších efektů je [[průjem]], který rezultuje z narušené rovnováhy [[střevo|střevní]] flóry, "dobrých bakterií", které přebývají v zažívacím systému člověka. Jiné vedlejší efekty mohou rezultovat z interakce mezi antibiotikem a jinými léky, např. zvýšený risk poškození [[šlacha|šlachy]] z užívání antibiotika Chinolon se systemickým [[kortikosteroid]]em. |
== Nesprávné použití antibiotik == | == Nesprávné použití antibiotik == | ||
| Řádka 117: | Řádka 118: | ||
== Nad antibiotiky == | == Nad antibiotiky == | ||
| − | Naneštěstí podobná snadnost nalezení sloučenin, které bezpečně léčí bakteriální infekce se ukázala být mnohem složitější s ohledem na plísňové a virové infekce. Antibiotický výzkum vedl k velkým krokům v našem poznání základní biochemie a k současnému biologickému progresu, ale v praxi bylo objeveno, že susceptibilita (citlivost) bakterií na mnoho sloučenin, které jsou bezpečné pro lidi, je založena na důležitých rozdílech mezi [[buňka|buněčnou]] a molekulární [[fyziologie|fyziologií]] | + | Naneštěstí podobná snadnost nalezení sloučenin, které bezpečně léčí bakteriální infekce se ukázala být mnohem složitější s ohledem na plísňové a virové infekce. Antibiotický výzkum vedl k velkým krokům v našem poznání základní biochemie a k současnému biologickému progresu, ale v praxi bylo objeveno, že susceptibilita (citlivost) bakterií na mnoho sloučenin, které jsou bezpečné pro lidi, je založena na důležitých rozdílech mezi [[buňka|buněčnou]] a molekulární [[fyziologie|fyziologií]] bakteriových buněk a buněk savců. Ale i když jsou jasné velké rozdíly mezi plísněmi a lidmi, základní biochemie plísňové a savčí buňky je mnohem víc podobná a to natolik, že je málo terapeutických možností pro sloučeniny atakovat plísňové buňky bez poškození lidských buněk. Podobně víme, že viry reprezentují minimálního nitrobuněčného parazita, redukovaného na nemnoho genů DNA nebo RNA a s minimální molekulovou výbavu nutnou na proniknutí do buňky a ovládnutí mechanismu buňky na produkci nových virů. Proto mnoho virové metabolické biochemie není jen podobné na lidskou biochemii, ale to reálně je lidská biochemie a možné cíle antivirových sloučenin jsou omezeny na relativně málo složek samotného viru. |
==Externí linky (anglicky)== | ==Externí linky (anglicky)== | ||
Aktuální verze z 22. 10. 2017, 19:20
|
Antibiotika jsou léky ničící nebo zpomalující růst bakterií. Antibiotika tvoří jednu třídu "antimikrobiálních léků" (antimikrobiotika nebo též bakteriostatika), větší skupina kterých též obsahuje antivirotika, antiplísňové a antiparazitické léky. Jsou relativně neškodné pro hostitele a proto mohou být použity na léčbu infekcí. Termín "antibiotika" původně označoval jen formy antibiotik odvozených ze živých organismů, ale teď je aplikován i na syntetické antimikrobiotika, např. sulfonamidy. Antibiotika jsou malé molekuly s molekulární hmotností méně než 2000 a nepatří mezi enzymy.
Na rozdíl od předešlých způsobů léčby infekcí, které obsahovali otravy jako strychnin, antibiotika byli označeny jako "magické tablety" - léky zasahující nemoc bez poškození pacienta. Antibiotika nejsou efektivní u virových, plísňových a jiných nebakteriálních infekcí a jednotlivé antibiotika jsou značně odlišné ve své účinnosti na různé typy bakterií. Některé specifické antibiotika (zvané "úzko-spektrální antibiotika") zasahují buď gram-negativní nebo gram-pozitivní bakterie a jiné jsou víc širokospektrální antibiotika. Účinnost jednotlivých antibiotik se mění podle lokality infekce a schopnosti antibiotika dosáhnout dané místo. Orální (užívané ústně) antibiotika jsou nejlepším řešením, jsou-li účinné a nitrožilní antibiotika se používají ve vážnějších případech. Antibiotika mohou být někdy aplikovány místně, např. jako oční kapky nebo mast.
Historie
Následujíc dřívější experimenty, které ukázaly zajímavé antibakteriální účinky z různých bakteriálních sekretů, německý vědec E. de Freudenreich izoloval v roce 1888 bakteriální sekreci a zaznamenal její antibakteriální vlastnosti. Pyocyanáze vylučována bacilem "Bacillus pyocyaneus" zpomalila růst jiných bakterií v okolí a byla toxická pro mnoho bakterií způsobujících nemoc. Naneštěstí vlastní toxicita pyocyanázy a její nestabilní charakter neumožnil její použití jako účinného bezpečného antibiotika v lidském těle.
První účinné objevené antibiotikum byl penicilin. Francouzský doktor Ernest Duchesne zaznamenal v roce 1896 tezi, že určité plísně druhu Penicilium ničí bakterie. Duchesne skonal během několika let a jeho výzkum byl zapomenut po generaci, až do přispění náhody. Alexander Fleming pěstoval bakterie na agarových plotnách a jedna z nich byla napadena náhodní plísňovou kontaminací. Fleming zaznamenal čistou zónu kolem kolonie plísně. Protože Fleming předtím studoval schopnost enzymu lysozym ničit bakterie, teď pochopil, že plíseň vylučovala něco, co zastavilo růst bakterií. Věděl, že tato látka může mít obrovský užitek pro medicínu. I když nebyl schopen rafinovat (očistit) sloučeninu (kruh beta-laktam v penicilinové molekule nebyl stabilní po vyzkoušených rafinačních metodách), popsal objev ve vědecké literatuře v roce 1929. Protože plíseň byla druhu Penicilium, nazval tuto sloučeninu penicilin.
V 30. letech 20. století německý výzkumník Gerhard Domagk zkoumal antibakteriální vlastnosti některých barviv. Jedním z nich byl sulfonamid, prontosil, který se ukázal být účinným proti infekcím u lidí pro svoji proměnu v hostitelu na aktivní formu - sulfanilimid. Podle současné širší definice to možno asi kvalifikovat jako první úspěšné použití orálního (ústního) antibiotika. Po nějaké době Rene Dubos izoloval tyrotricin - antibiotikum používané místně na kožní infekce z půdních bakterií.
Pro zvýšenou potřebu léčby infekcí z ran ve 1940-tych letech bylo mnoho prostředků vloženo do výzkumu a rafinace penicilinu a team, který vedl Howard Walter Florey, úspěšně vyprodukoval použitelná množství rafinované aktivní složky, která byla rychle testována na klinických případech. Doktoři byli překvapeni z rychlé a spolehlivé léčby stavů, které do té doby byly těžce léčitelné a často fatální. Výzkum dalších druhů plísní a jiných organismů ukázal až dosud neznámou úrověň chemického boje proti bakteriím. Nové antibiotika byly rychle objevovány a začali se široce používat. Nová éra výzkumu podobných "magických" chemoterapeutických léčiv pro jiné nemoci eventuálně vedla k úspěchům v rakovinové chemoterapii.
Objev antibiotik spolu s anestezií a aplikací hygienických praktik u doktorů (např. mytí rukou a použití sterilizovaných instrumentů) značně inovoval medicínu. Považuje se za největší progres pro zdraví od moderní kanalizace. Lidé v rozvojových zemích si těžko dovedou představit, že jedno škrábnutí vždy nese risk infekce a skonu.
Klasifikace
Je mnoho způsobů klasifikace antibiotik.
Jedna z klasifikací je podle chemické struktury:
- Aminoglykosidy
- Antibiotika kruhu Beta-laktam
- Carbapenemy
- Cefalosporiny a cefamyciny
- Monocyklické beta-laktamy
- peniciliny
- Glykopeptidové antibiotika
- Oxazolidinony
- Linezolid
- Chinupristin/dalfopristin
- Polyketidy
- Polymyxiny
- Chinolony (fluorochinolony)
- Nalidixická kyselina
- Ciprofloxacin (Cipro)
- Ofloxacin
- Norfloxacin (Norflox)
- Levofloxacin (Levaquin)
- Trovafloxacin (Trovan)
- Streptograminy
- Sulfonamidy
- Jiné důležité antibiotika:
Další klasifikace je podle mechanismu jejich účinku (tedy podle mechanismu kterým selektivně ničí bakteriové buňky):
- Antibiotika, které interferují (zasahují) v syntéze buněčné stěny
- Beta-laktamy, včetně penicilinů a cefalosporinů; mono-laktamy, např. Imipenem; vancomycin, bacitracin
- Antibiotika, které interferují s baktériální proteinovou syntézou
- Antibiotika, které se váží na ribozomální jednotku 50S
- Lincosamidy/lincosidy včetně clindamycinu a lincomycinu; chloramfenikol, makrolidy
- Antibiotika, které interferují s ribozomální jednotkou 30S
- Tetracykliny; aminoglykosidy včetně gentamicinu
- Antibiotika, které se váží na ribozomální jednotku 50S
- Léky, které inhibují folátovou syntézu
- Sulfonamidy a trimetoprim
- Léky, které interferují se syntézou DNA
- Metronidazol, chinolony, novobiocin
- Léky, které interferují se syntézou RNA
- Rifampin (rifampicin)
- Léky, které interferují s funkcí buněčné membrány
- Polymyxin B, gramicidin
Antibiotika mohou být též klasifikovány podle organismů, proti kterým jsou účinné a podle typu infekce, ve které jsou užitečné, co závisí na citlivosti organismů, které nejčastěji způsobují infekce a na koncentraci antibiotika v postihnuté tkáni.
Vedlejší efekty
Vedlejší efekty jsou v rozsahu od slabé bolesti hlavy po vážné alergické reakce. Jeden z častějších vedlejších efektů je průjem, který rezultuje z narušené rovnováhy střevní flóry, "dobrých bakterií", které přebývají v zažívacím systému člověka. Jiné vedlejší efekty mohou rezultovat z interakce mezi antibiotikem a jinými léky, např. zvýšený risk poškození šlachy z užívání antibiotika Chinolon se systemickým kortikosteroidem.
Nesprávné použití antibiotik
Obvyklé formy chybného použití antibiotik zahrnují užívání nesprávného antibiotika, zvláště užití antibakteriálních typů pro virové infekce jako rýma a nedodržení užití celé předepsané dávky antibiotik, obvykle pro pacientův subjektivní pocit zlepšení předtím, než jsou infikující organismy kompletně eliminovány. Kromě selhání léčby mohou tyto praktiky rezultovat do antibiotické rezistence (odolnosti vůči účinkům antibiotik).
V USA je velké množství antibiotik běžně obsaženo v malých dávkách v potravě pro zdravá zvířata na farmách, protože tato praxe prokazatelně způsobuje rychlejší růst zvířat. Oponenti této praxe ale poukazují na pravděpodobnost, že to též vede k antibiotikové rezistenci, často u bakterií, o kterých se ví, že též infikují lidi, i když zatím existuje malá nebo žádná prokazatelnost podobného transferu antibiotické rezistence.
Antibiotická rezistence
Jedním z vedlejších efektů chybného užívání antibiotik je vývoj antibiotické rezistence infikujících organismů, podobné vývoji pesticidové rezistence u hmyzu. Evoluční teorie genetické selekce vyžaduje, aby téměř 100% infikujících organismů bylo zničeno pro prevenci genetické selekce na rezistenci. Přežije-li malá část populace bakterií léčbu a může-li se reprodukovat, průměrná susceptibilita (citlivost) nové populace na ničící sloučeninu bude mnohem menší než u původní populace, protože nová populace vyrostla z nemnohých organismů, které vydrželi původní léčbu. Toto přežití často rezultuje z dědičné rezistence na sloučeninu, která byla řídká v původní populaci, ale teď je mnohem víc častá u potomstva úplně selektovaného z těchto původně málo rezistentních organismů.
Antibiotická rezistence se stala vážným problémem v rozvojových i vyspělých zemích. V roce 1984 polovině lidí v USA způsobil aktivní tuberkulózu kmen, který byl rezistentní na aspoň 1 antibiotikum. V některých zařízeních jako nemocnice a střediska pro děti je míra antibiotikové rezistence natolik vysoká, že obyčejné levné antibiotika jsou prakticky zbytečné na léčbu častých infekcí. To vede k častějšímu použití nových a drahších sloučenin, co obratem vede k dalšímu zvýšení rezistence na tyto nové léky a k nekončící snaze vyvinout nové a odlišné antibiotické následovníky pro udržení předstihu před infekcemi. Existují obavy, že lidé eventuálně ztratí tento předstih a doba, kdy neměli obavu z fatálních bakteriálních infekcí bude jen vzpomínkou.
Dalším příkladem selekce je Stafylokok aureus, který byl úspěšně léčen penicilinem v 40. a 50. létech 20. století. V současnosti jsou téměř všechny kmeny rezistentní na penicilin a mnoho je rezistentních na nafcilin, nechávajíc jen úzký výběr léků jako vancomycin pro účinnou léčbu. Situaci zhoršuje fakt, že geny kódující antibiotickou rezistenci mohou být přenášené mezi baktériemi, umožňujíc tím baktériím, které nikdy nebyli vystaveny působení antibiotik získat rezistenci od těch, které ji mají. Problém antibiotické rezistence se zhorší, když antibiotika jsou použity na léčbu nemocí, u kterých nemají žádný účinek, např. rýma nebo jiné virové nemoci a když jsou široce používány na prevenci a ne léčbu (např. v potravě pro zvířata), protože to víc baktérií vystaví selekci pro rezistenci.
Nad antibiotiky
Naneštěstí podobná snadnost nalezení sloučenin, které bezpečně léčí bakteriální infekce se ukázala být mnohem složitější s ohledem na plísňové a virové infekce. Antibiotický výzkum vedl k velkým krokům v našem poznání základní biochemie a k současnému biologickému progresu, ale v praxi bylo objeveno, že susceptibilita (citlivost) bakterií na mnoho sloučenin, které jsou bezpečné pro lidi, je založena na důležitých rozdílech mezi buněčnou a molekulární fyziologií bakteriových buněk a buněk savců. Ale i když jsou jasné velké rozdíly mezi plísněmi a lidmi, základní biochemie plísňové a savčí buňky je mnohem víc podobná a to natolik, že je málo terapeutických možností pro sloučeniny atakovat plísňové buňky bez poškození lidských buněk. Podobně víme, že viry reprezentují minimálního nitrobuněčného parazita, redukovaného na nemnoho genů DNA nebo RNA a s minimální molekulovou výbavu nutnou na proniknutí do buňky a ovládnutí mechanismu buňky na produkci nových virů. Proto mnoho virové metabolické biochemie není jen podobné na lidskou biochemii, ale to reálně je lidská biochemie a možné cíle antivirových sloučenin jsou omezeny na relativně málo složek samotného viru.
Externí linky (anglicky)
- Antibiotic News from Genome News Network (GNN)
- Are Antibiotics Killing Us? -Discover Magazine
- JAAPA: New antibiotics useful in primary care
- A new method for controlling bacterial activity without antibiotics - Research conducted at the Hebrew University
- BURDEN of Resistance and Disease in European Nations
- Alliance for the Prudent Use of Antibiotics